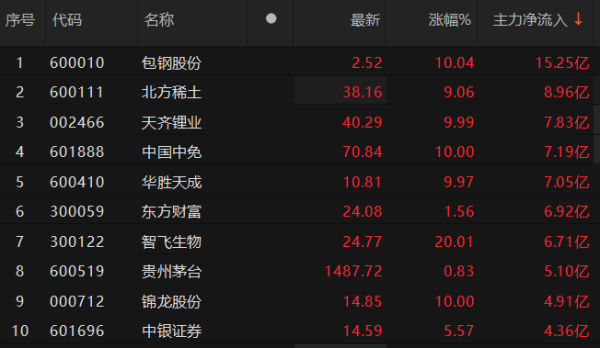
长春高新晚间公告,控股子公司金赛药业收到国家药品监督管理局核准签发的《受理通知书》信德,金赛药业GS3-007a干混悬剂境内生产药品注册临床试验申请获得受理,该药品适应症为用于因内源性生长激素缺乏所引起的儿童生长缓慢。
举报 相关阅读 中国澳门启动首个新药临床试验
中国澳门启动首个新药临床试验这次临床试验启动意味着粤港澳大湾区临床研究网络“最后一块拼图”得以补齐。
41 08-29 17:38 半年盘点|中国脑机接口进入临床试验,拓展消费级应用场景
半年盘点|中国脑机接口进入临床试验,拓展消费级应用场景中国的研究者正在多个方向推动脑机接口领域的进展,例如改进解码神经数据的算法和植入设备。同时信德,政府也已将脑机接口列为优先扶持的创新领域,投资机构大量资金争相涌入该领域。
6 525 07-11 13:18 去年我国新药临床试验数量再创新高,司美格鲁肽领跑
去年我国新药临床试验数量再创新高,司美格鲁肽领跑2024年,我国新药注册临床试验数量为近五年新高,将近5000项(4900项),较上一年增长了13.9%。
9 649 06-20 10:52 创新药临床试验审评审批提速,一类创新药等纳入30日通道
创新药临床试验审评审批提速,一类创新药等纳入30日通道此次征求意见稿,拟统一符合资质要求的药物范畴,并在“生物制品1类创新药”的基础上,还明确纳入符合要求的“中药”“化学药品”。
481 06-16 18:11 科创板新增受理1家未盈利企业IPO申请,有何信号?
科创板新增受理1家未盈利企业IPO申请,有何信号?目前共有11家未盈利企业在IPO审核过程中信德。
IPO动态 111 06-15 11:16 一财最热 点击关闭股升网配资提示:文章来自网络,不代表本站观点。
沪深京指数
热点资讯